

李翠笛老师等开发组装共递送系统的3D打印支架激活吞噬骨肿瘤的巨噬细胞
近日,李翠笛老师等在Biomaterials杂志上发表了一篇题为“Activation of bone tumor-eating macrophages via assembling and co-delivering 3D printed scaffold”的研究论文。该研究开发了一种阶段性激活局部肿瘤吞噬巨噬细胞并促进骨组织再生的多功能核壳结构治疗植入物,为骨肿瘤术后抑制肿瘤免疫逃逸并促进骨组织修复的治疗方案提供了新的工程化策略。
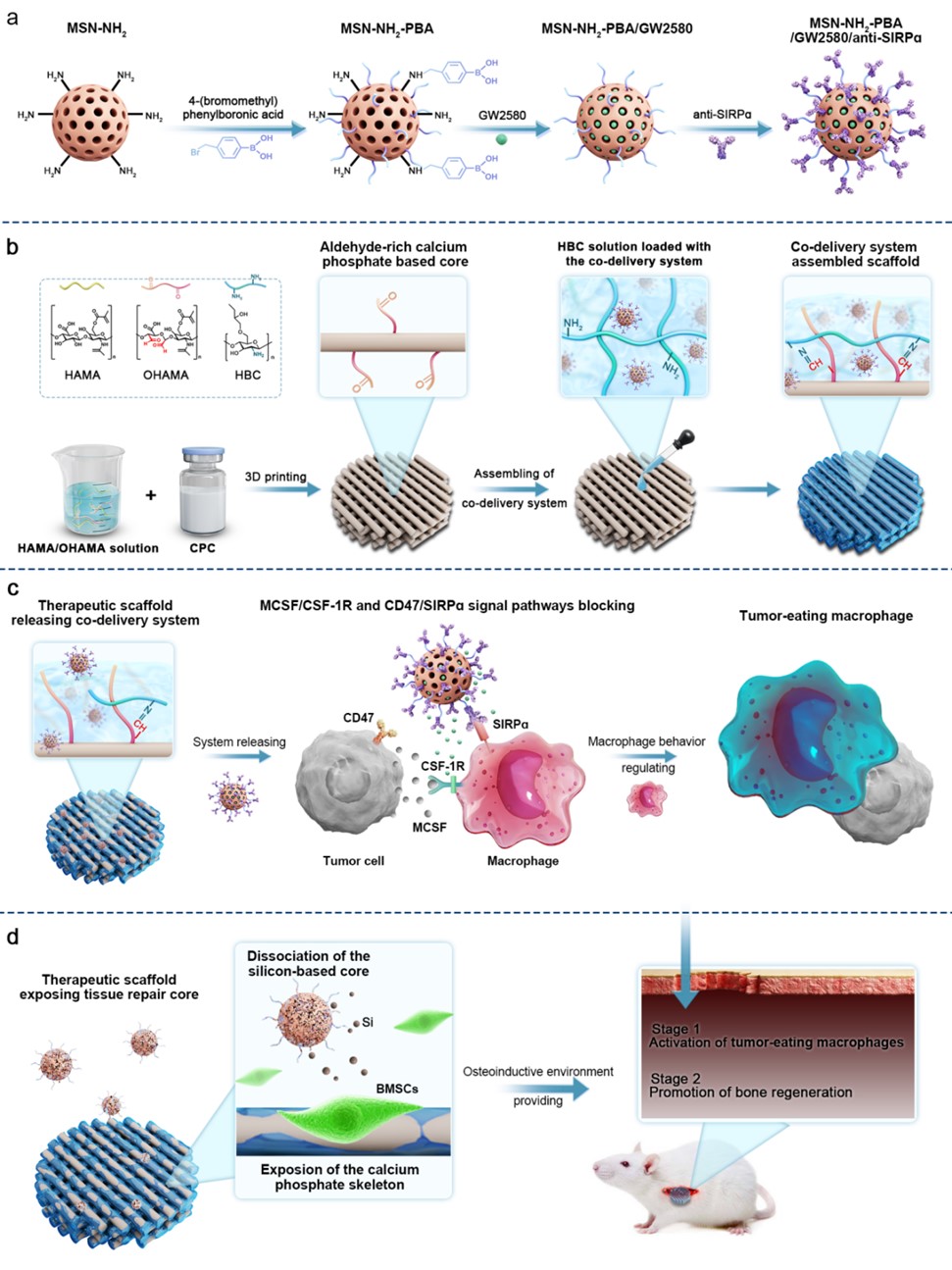
图1:共递送系统组装植入物的制备及其在骨肿瘤术后治疗中的作用机制
恶性骨肿瘤手术切除后存在复杂的大段骨缺损需要修复,伴随着复发后生存率低的挑战。开发用于修复个体化骨缺损和抑制肿瘤复发的治疗性植入物对于提高患者生存率和生活质量至关重要。3D打印磷酸钙植入物具有高度可设计的内外部结构和稳定骨引导性能,能够有效填补复杂骨缺损并促进组织修复,目前尚缺乏抑制肿瘤复发功能。研究表明,肿瘤细胞过量分泌巨噬细胞集落刺激因子(MCSF)并表达“别吃我”信号CD47,从而诱导巨噬细胞M2极化并使其丧失吞噬能力是肿瘤免疫逃逸并复发的关键因素。因此,将靶向MCSF/CSF-1R和CD47/SIRPα信号轴的双通路阻断递送系统整合到3D打印磷酸钙植入物中,有潜力增强局部巨噬细胞肿瘤吞噬功能,从而抑制肿瘤复发。
基于此,本研究设计将疏水CSF-1R通路抑制剂富集在苯硼酸修饰的介孔二氧化硅纳米载体(MSN-NH2-PBA)内部多孔结构中,基于硼氮配位键将SIRPα抗体固载在其表面构建药物靶向共递送系统,并利用动态共价键将递送系统组装于富含醛的3D打印磷酸钙支架上,开发了一种阶段性激活局部肿瘤吞噬巨噬细胞并促进骨组织再生的多功能核壳结构治疗植入物。体外研究表明共递送系统能有效结合于单核细胞/巨噬细胞表面阻断相关通路,从而显著抑制骨髓来源单核细胞的M2极化,并增强巨噬细胞对肿瘤细胞的吞噬能力;共递送系统可以从核壳结构植入物中逐渐释放,同时保持其对巨噬细胞的调控功能。在体内肿瘤治疗模型中,治疗植入物显著减少了局部M2巨噬细胞并抑制了肿瘤生长。在正常小鼠皮下植入8周后,治疗植入物表现出良好的生物相容性,并促进了均匀的骨生长。本研究为骨肿瘤术后抑制肿瘤免疫逃逸并促进骨组织修复的治疗方案提供了新的工程化策略。
期刊页码:Biomaterials. 2026, 324:123495
原文链接:https://doi.org/10.1016/j.biomaterials.2025.123495